无我,无界,有物
发表时间:2022-05-20 22:44
一个科技领域的孕育与发展,要三个方面,第一是有人全心投入,第二是有人自由探索,第三是有人创造器物。这三个方面的恰当顺序是,先无我,再无界,最后才有物。我们过去在洗涤菌群移植领域的十年,正是如此。张发明图注:中国菌群移植平台CMTS证据改变医学实践2022年5月,Microbial Biotechnology期刊在线发表了中国菌群移植平台(CMTS)自2012年至2021年从粪菌移植到洗涤菌群移植的方法学发展过程,分析洗涤菌群移植体系的建立及其对方法学、计量和移植途径的影响。 研究生陆高辰、汪韦宏为共同第一作者,通讯作者张发明,作者名单还有多年为中国菌群移植平台建设和发展做出重要贡献的李潘、温泉、崔伯塔。 粪菌移植(fecal microbiota transplantation,FMT)是重建肠道微生态的有效手段。特别是在近10年,全球科学家和医生经历从重视人体微生物的独立价值到重视微生态的整体贡献的认识转变,为探索疾病发生机制及其诊治新方法带来了变革性机会。“FMT”由美国FMT合作组于2011年正式定名,2012年译为“粪菌移植”作其中文学术名词,尽管“粪菌移植”已经从名词学上代替原始手工的“粪便移植”成为学术交流常规使用的专业名词,然其操作技术本质上在欧美的使用和中国古人所用的方法无异。因此,将疗效很好但又粗糙的技术做到极致,成为全球医学发展的强烈需求。张发明团队在Microbial Biotechnology期刊发表的论文介绍其过去10年建立中国菌群移植平台(China Microbiota Transplantation System, CMTS)的历程。自2012年开始建立用于临床研究的医院粪菌库,后于2015年成为国家消化系统病临床医学研究中心(西安)的核心项目,命名为中华粪菌库(Chinese fmtBank),旨在为全国难治性肠道感染患者提供非营利性粪菌移植异地救援。2017年,国家消化系统病临床医学研究中心支持中华粪菌库升级为中国菌群移植平台,服务于全国菌群移植医疗和科研,集临床服务、数据管理和新技术研究为一体(图1),并在线实时提供菌群移植长期随访的安全性数据(http://fmtbank.org),微信号为“菌群平台”。 图1 中国菌群移植平台的框架和实验室
图1 中国菌群移植平台的框架和实验室
中国菌群移植平台的核心技术从无到有,经历如下发展历程:2014年,团队研制出世界上第一套智能粪菌分离系统(GenFMTer)投入实验室运行。2015年,团队发明了结肠途径经内镜肠道植管术(transendoscopic enteral tubing, TET)。粪菌移植的方法改变带来的安全性提升,成为临床应用显而易见的事实,团队据此深入研究,回答其中的科学机制,提出洗涤菌群移植(washed microbiota transplantation, WMT)的全新概念,即基于智能化粪菌分离系统及严格质控相关漂洗和移植途径的全流程技术。洗涤菌群移植的概念、理论机制于2019年在Protein & Cell被发表,入选期刊封面,并成为高被引论文。2019年,张发明牵头组织中国两岸三地15座城市28名专家组成专家委员会,以“粪菌移植标准化研究小组”的集体名义,按国际共识的严格流程制定“洗涤菌群移植方法学共识”,2019年12月12日完成最后面对面讨论和最后一轮投票,确立为《洗涤菌群移植南京共识》。2020年在Chinese Medical Journal发表,成为全球该领域高度关注和高频引用的共识。 自2014年以来,团队开始招募并匿名使用与患者无亲缘关系的供体。候选筛查包括:问卷筛查(卷筛)、面对面筛查(面筛)、实验室筛查(验筛)和监查筛查(监筛)。2014年至2021年间,共收回有效问卷1036份(95.1%,1036/1089),供体筛选合格率为3.1%(图2)。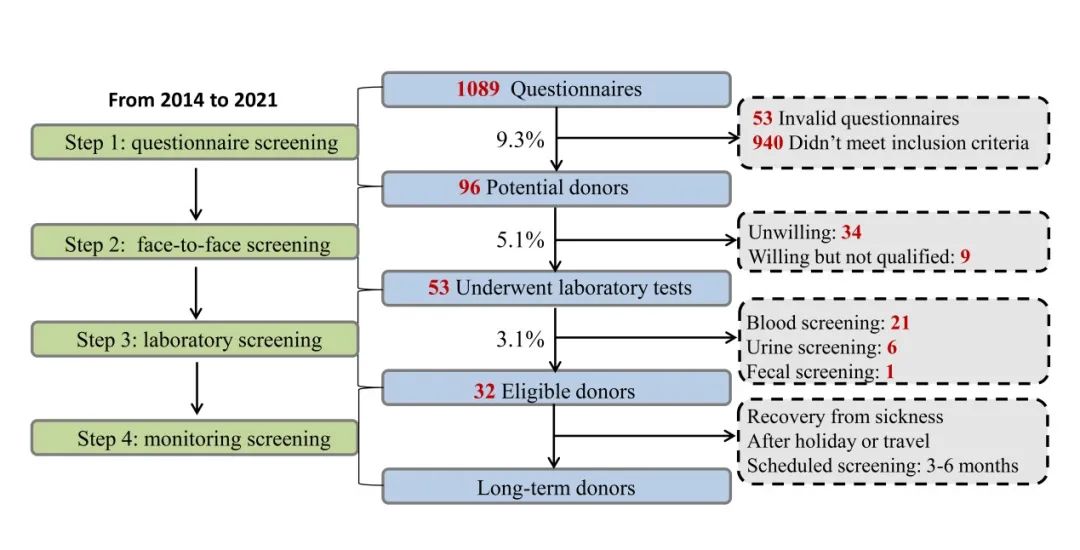 本研究的数据分析再次强调团队此前定义的计量方法(unit,简称U,1U含1.0×1013个细菌),分析执行该标准的结果和意义。一般为成人和7岁以上儿童单次使用5U,7岁以下儿童根据病情单次使用1-5U,这样以最少移植次数获得最大程度疗效,节省住院时间和医疗费用。
本研究的数据分析再次强调团队此前定义的计量方法(unit,简称U,1U含1.0×1013个细菌),分析执行该标准的结果和意义。一般为成人和7岁以上儿童单次使用5U,7岁以下儿童根据病情单次使用1-5U,这样以最少移植次数获得最大程度疗效,节省住院时间和医疗费用。 本研究还分析了本中心分离菌群的方法与全球其他粗糙方法的差异,特别提出高度利用宝贵的合格粪便资源,将100g设限更改为50g,并提供了洗涤制备富集菌群数量的证据。否定了过去多个共识和指南中建议100g作为制备标准(图3和图4)。
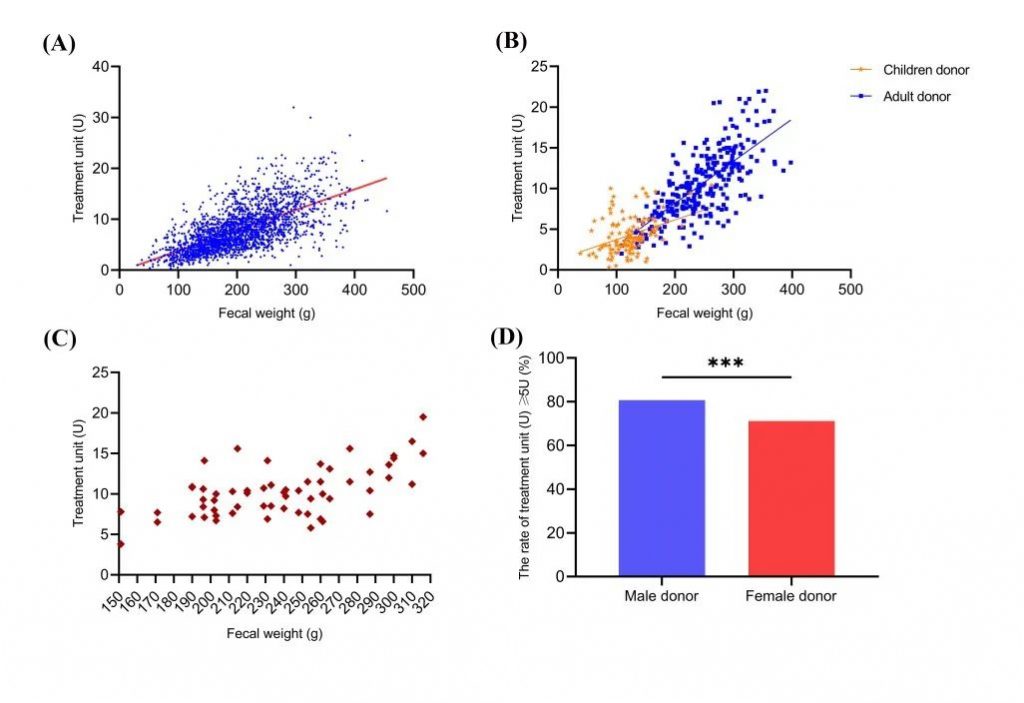 图3 供体粪便重量与洗涤富集菌群数量的相关性
图3 供体粪便重量与洗涤富集菌群数量的相关性
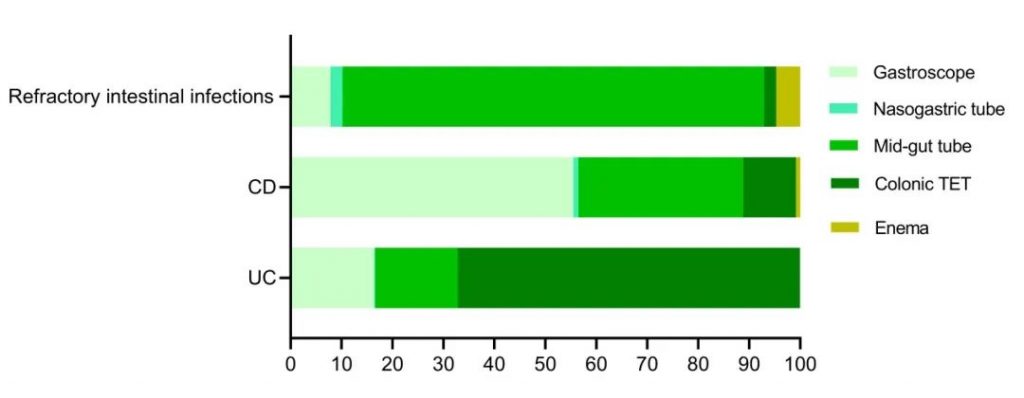
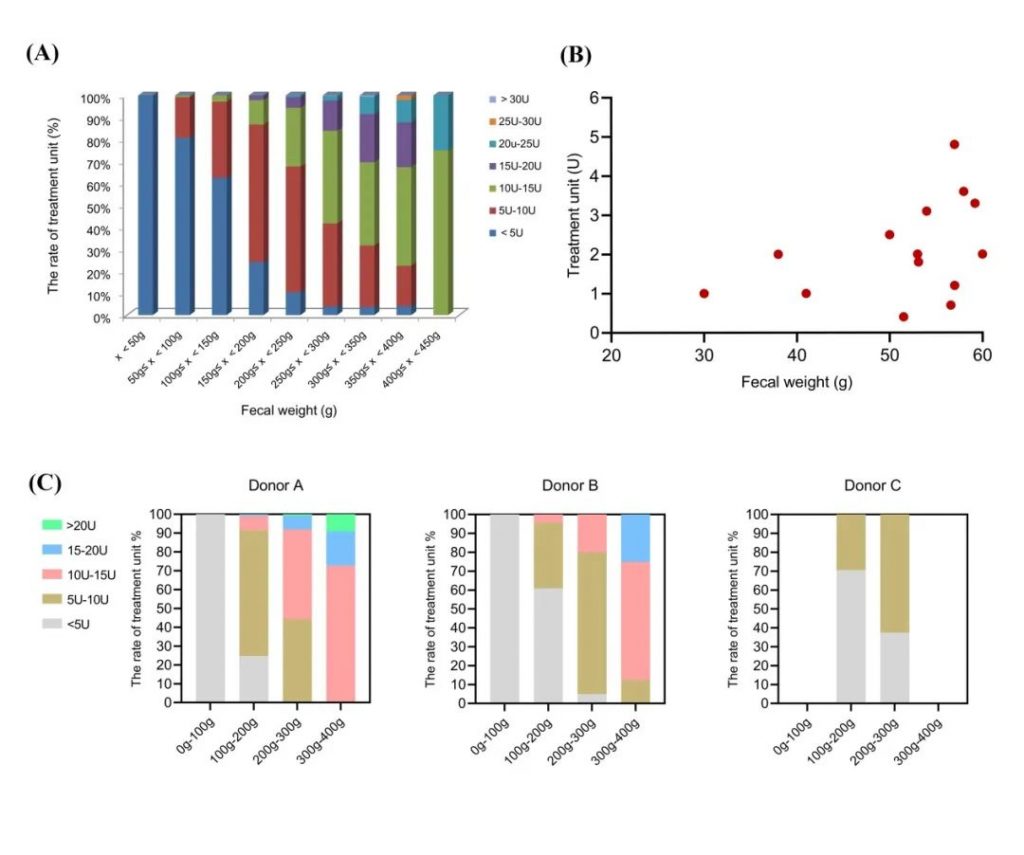 图4 供体粪便重量的分布及治疗量产出 本研究分析强调,对于需要多次WMT治疗或结肠给药(免疫抑制剂、激素、肠内营养等)联合WMT治疗的患者,推荐使用经内镜肠道植管术(transendoscopic enteral tubing, TET)途径,尤其是结肠TET途径(图5)。TET途径优势明显:(1)使用手工制备时,会发生堵塞管腔,而洗涤菌群制备则不会出现堵管;(2)手工制备粪菌悬液体积变化大,有效剂量不定,对移植途径的考量有冲突,而洗涤菌群移植是以洗涤富集所得的菌群为基础的,移植途径不影响剂量选择;(3)可重复的结肠TET途径,兼顾抽吸减压引流治疗肠梗阻或肠穿孔,满足动态采集近端结肠回盲部标本用于检验和研究。图5 UC、CD和难治性肠道感染患者的不同移植途径 本研究强调,最新数据显示,洗涤菌群移植使溃疡性结肠炎(ulcerative colitis, UC)患者的不良事件(adverse event, AE)发生率下降80%,并且使UC患者中最常见的发热发生率下降86%。这进一步刷新了本团队2019年报道的73%的数据记录(图6)。图6 洗涤菌群移植降低移植相关不良事件发生率此前,本团队联合美国、欧洲专家共同提出评价粪菌移植安全性的分类概念,按照术后1个月为分界,1月以内为短期不良事件,1月以上为长期不良事件。本研究进一步分析强调,关注短期不良事件发生率,特别是基于溃疡性结肠炎、重症感染和造血干细胞移植等肠黏膜屏障受损人群的数据更具说服力,而基于肠黏膜屏障完整疾病(如便秘、自闭症、肠易激综合征等)的安全性数据说服力非常有限。值得强调的是,移植后发热事件的发生,有人误解为“治疗显效”,这是错误的认识。 本研究通过报告中国菌群移植平台洗涤菌群移植体系建立与质量控制的成果,推动粪菌移植由手工制备进入洗涤菌群移植时代,以改变菌群移植在临床实践,特别是实验方法学、计量方法、安全性、移植途径以及相关的临床决策。这是《洗涤菌群移植南京共识》发表之后本领域方法学研究的又一重要进步。致谢:社会公益捐款(肠病研究基金、南京医科大学樊代明整合医学研究基金)、国家自然科学基金、国家消化系统疾病临床医学中心长期为本研究团队就洗涤菌群移植体系的自由探索提供至关重要的资助。原文链接:
图4 供体粪便重量的分布及治疗量产出 本研究分析强调,对于需要多次WMT治疗或结肠给药(免疫抑制剂、激素、肠内营养等)联合WMT治疗的患者,推荐使用经内镜肠道植管术(transendoscopic enteral tubing, TET)途径,尤其是结肠TET途径(图5)。TET途径优势明显:(1)使用手工制备时,会发生堵塞管腔,而洗涤菌群制备则不会出现堵管;(2)手工制备粪菌悬液体积变化大,有效剂量不定,对移植途径的考量有冲突,而洗涤菌群移植是以洗涤富集所得的菌群为基础的,移植途径不影响剂量选择;(3)可重复的结肠TET途径,兼顾抽吸减压引流治疗肠梗阻或肠穿孔,满足动态采集近端结肠回盲部标本用于检验和研究。图5 UC、CD和难治性肠道感染患者的不同移植途径 本研究强调,最新数据显示,洗涤菌群移植使溃疡性结肠炎(ulcerative colitis, UC)患者的不良事件(adverse event, AE)发生率下降80%,并且使UC患者中最常见的发热发生率下降86%。这进一步刷新了本团队2019年报道的73%的数据记录(图6)。图6 洗涤菌群移植降低移植相关不良事件发生率此前,本团队联合美国、欧洲专家共同提出评价粪菌移植安全性的分类概念,按照术后1个月为分界,1月以内为短期不良事件,1月以上为长期不良事件。本研究进一步分析强调,关注短期不良事件发生率,特别是基于溃疡性结肠炎、重症感染和造血干细胞移植等肠黏膜屏障受损人群的数据更具说服力,而基于肠黏膜屏障完整疾病(如便秘、自闭症、肠易激综合征等)的安全性数据说服力非常有限。值得强调的是,移植后发热事件的发生,有人误解为“治疗显效”,这是错误的认识。 本研究通过报告中国菌群移植平台洗涤菌群移植体系建立与质量控制的成果,推动粪菌移植由手工制备进入洗涤菌群移植时代,以改变菌群移植在临床实践,特别是实验方法学、计量方法、安全性、移植途径以及相关的临床决策。这是《洗涤菌群移植南京共识》发表之后本领域方法学研究的又一重要进步。致谢:社会公益捐款(肠病研究基金、南京医科大学樊代明整合医学研究基金)、国家自然科学基金、国家消化系统疾病临床医学中心长期为本研究团队就洗涤菌群移植体系的自由探索提供至关重要的资助。原文链接:https://sfamjournals.onlinelibrary.wiley.com/doi/10.1111/1751-7915.14074
作者:陆高辰 汪韦宏

 图1 中国菌群移植平台的框架和实验室
图1 中国菌群移植平台的框架和实验室 图3 供体粪便重量与洗涤富集菌群数量的相关性
图3 供体粪便重量与洗涤富集菌群数量的相关性 图4 供体粪便重量的分布及治疗量产出
图4 供体粪便重量的分布及治疗量产出